EPO (Erythropoietin)
Blutdoping wurde erstmals 1988 auf die IOC-Liste der verbotenen Methoden gesetzt. Mit dieser Methode wurde versucht, die Gesamtzahl an roten Blutkörperchen (Erythrozythen) zu erhöhen, um eine größere Menge an Sauerstoff transportieren zu können. Damit einhergehend soll die Ausdauerleistung verbessert werden. Mit dem gentechnisch produzierten EPO können die gleichen Effekte erreicht werden wie mit dem Blutdoping, so dass die aufwendige und auch gefährliche Methode der Bluttransfusion vermieden werden kann.
EPO gehört zur Gruppe der Glycoproteine. Hierunter werden Eiweißmoleküle (Proteine) verstanden, die mit Kohlenhydratketten verknüpft sind. EPO hat ein Molekulargewicht von ca. 30.000, wobei die Proteinkette aus insgesamt 165 Aminosäuren besteht. An vier stellen des Proteins erfolgt eine Bindung mit komplex aufgebauten Kohlenhydraten. Diese Kohlenhydratketten sind unbedingte Voraussetzung für die biologische Aktivität der Verbindung. Der Kohlenhydratanteil beträgt ca. 40% des Gesamtmoleküls.
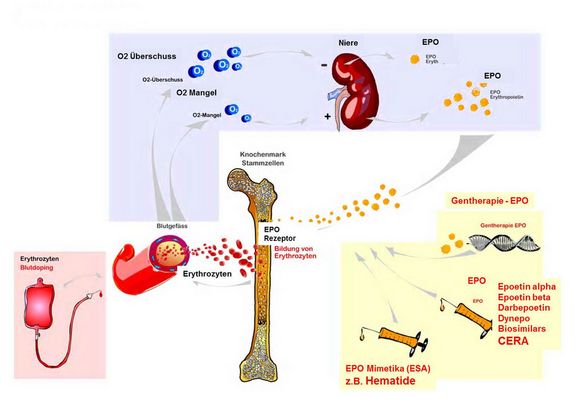
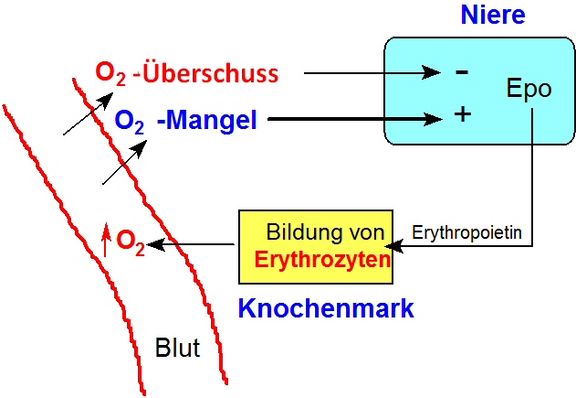
EPO wird vorwiegend in der Niere gebildet und stimuliert in den Knochenmark-Stammzellen die Ausreifung der Erythrozyten.
Dieses führt zu einer Erhöhung der Bildungsrate an Erythrocyten, die in ihrer ersten Zeit noch als Reticulozyten bezeichnet werden. Die medizinische Anwendung von EPO erfolgt bei Patienten, die selber nicht mehr genügend EPO produzieren und somit zu wenig rote Blutkörperchen aufweisen, z.B. bei renaler Anämie oder bei Dialysepatienten.
Seit 1988 wird EPO gentechnisch hergestellt, wobei gentechnisch veränderte Säugetierzellen (Ovarienzellen chinesischer Hamster) verwendet werden. Das so produzierte EPO ist 100%ig identisch mit dem menschlichen EPO bezüglich der Aminosäuresequenz der Eiweißkette. Geringfügige Unterschiede bestehen aber in den Kohlenhydratanteilen, so dass hier eine Möglichkeit zur Differenzierung zum humanen EPO gesehen wird.
Weiterhin steht seit 1.Juni 2001 eine neue von Erythropoeitin abgeleitete Substanz, die die Erythropoese stimuliert, für die Behandlung der renalen Anämie zur Verfügung: Darbepoetin alfa (NESP, Novel Erythropoiesis Stimulating Protein, Aranesp®), ebenfalls von der Firma Amgen. Dieses neue Produkt unterscheidet sich vom bisherigen rekombinant hergestellten EPO dadurch, dass 5 Aminosäuren ausgetauscht und zusätzliche Zuckerketten in das Molekül eingefügt worden sind.
Damit erhöht sich die relative Molekülmasse von 30.400 auf 38.500 und der Zuckeranteil des bisherigen EPO von 40 auf 52% des gesamten Molekulargewichtes.Die Halbwertszeit von Darbepoetin (NESP) liegt bei ca. 21 h nach intravenöser Injektion während Erythropoietin eine Halbwertszeit von 8,5 h aufweist. Nach subkutaner Injektion (Injektion ins Hautgewebe) verlängert sich die Halbwertszeit auf ca. 49 h (27-89h) bzw. 16-24 h für Epoetin.
Weitere Informationen:
Manipulationen zur Verbesserung des Sauerstofftansportes
"Die Mehrzahl der Blutzellen oder Blutkörperchen wird im Knochenmark gebildet. Das Knochenmark selbst ist ein schwammartiges Gewebe, das sich in den großen Knochen des Körpers befindet. Im Erwachsenenalter findet die Blutbildung vor allem in den Knochen der Wirbelsäule, Hüfte, Schulter, Rippen, im Brustbein und in den Schädelknochen statt."
Zitat s. Webseite Kompetenznetz Leukämie
Literatur
Jelkmann W: Physiology and Pharmacology of Erythropoietin. Transfus Med Hemother 2013;40:302-309.
download
Clasing, Dirk. Doping: Erythropoetin – Medikament und Dopingmittel. Deutsches Ärzteblatt Studieren.de, SS 2007: 30.
download
Jelkmann W. Use of recombinant human erythropoietin as an antianemic and performance enhancing drug. Curr Pharm Biotechnol. 2000 Jul;1(1):11-31.
download